¿Has oído hablar de Machine Learning? ¿Y de las imágenes hiperespectrales?
"Estos conceptos pueden parecer sacados de una película de ciencia ficción, pero nada más alejado: son ciencia real, y en el proyecto NEMESIS-3D-CM se asocian para dar un paso más en la lucha contra el cáncer. Veamos primero de qué estamos hablando."
Cuando nos referimos a Machine Learning nos adentramos en las ciencias informáticas, dentro del campo de la inteligencia artificial. ¿Puede pensar una máquina? Mediante Machine Learning se crean algoritmos que enseñan a una máquina a desarrollar respuestas en base a un aprendizaje generado sobre datos suministrados previamente. Por ejemplo, si queremos que un sistema informático identifique la figura de un león de entre las figuras de otros animales, necesitamos crear un modelo a partir de un gran número de imágenes de un león, de forma que la computadora reconozca al animal en cualquier postura, tamaño o perspectiva. De esta manera “enseñamos” a pensar a una máquina, para que de forma autónoma nos proporcione valoraciones, respuestas e incluso predicciones a partir de información real y diferente de la utilizada hasta entonces.
¿Y qué hay de las imágenes hiperespectrales? Las imágenes que estamos acostumbrados a ver se generan con una parte pequeña del espectro electromagnético (lo que llamamos el espectro visible), la misma que nuestro ojo puede captar con el sentido de la vista y gracias a la cual distinguimos los colores. Sin embargo, la radiación electromagnética que la materia puede absorber, reflejar y transmitir es mucho más amplia. Las imágenes hiperespectrales se generan a partir de la radiación de centenas de bandas espectrales (visible, infrarrojo, ultravioleta) de forma. Que mediante sensores especializados podemos captar información sobre los objetos mucho más compleja que la proporcionada por una imagen estándar, en la que sólo se registran tres bandas de color (rojo, verde y azul). Podemos imaginar la elevada cantidad de datos que las imágenes hiperespectrales conllevan, reconstruyéndose como modelos tridimensionales que incluyen además información espacial, por lo que su procesamiento ha de hacerse usando métodos computacionales. La ciencia utiliza imágenes hiperespectrales en muy diversos campos: en el campo de la vegetación y mineralogía mediante satélites de teledetección, en el estudio de obras de arte y manuscritos antiguos, y también en el desarrollo de aplicaciones biomédicas. Precisamente, esta última utilidad es la que el proyecto NEMESIS-3D-CM aborda.

Profesionales de la salud usando el microscopio quirúrgico durante la cirugía
El proyecto NEMESIS-3D-CM, puesto en marcha por investigadores del CITSEM de la Universidad Politécnica de Madrid (UPM) y la Fundación de Investigación Biomédica del Hospital Universitario 12 de Octubre de Madrid, propone construir un sistema de diagnóstico basado en imágenes hiperespectrales y Machine Learning aplicable a la delimitación de tumores cerebrales durante las intervenciones quirúrgicas y ayudar así a los neurocirujanos en la toma de decisiones para la resección del tumor.
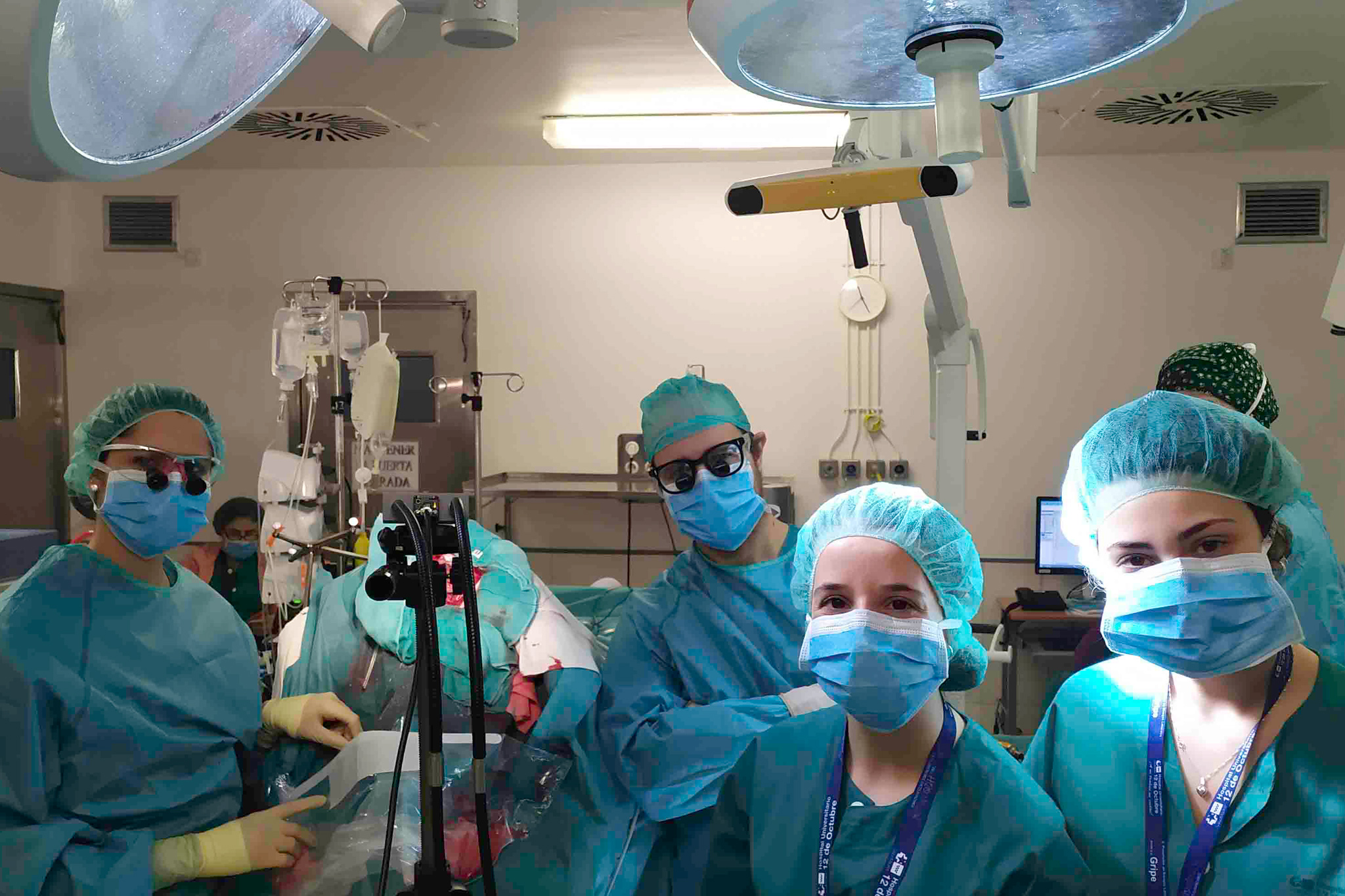
Grupo NEMESIS: investigadores y cirujanos trabajando in vivo
En el caso de los tumores, los cambios producidos por la malignización de las células hacen que las propiedades de absorción, dispersión y fluorescencia de los tejidos varía, siendo posible la obtención de información muy valiosa para el diagnóstico mediante el análisis de imágenes hiperespectrales. Estas imágenes, combinadas con valoraciones de anatomía patológica realizadas por especialistas, son la base del aprendizaje de un sistema computacional basado en Machine Learning, para el desarrollo de un dispositivo diagnóstico automatizado de uso quirúrgico.
Hemos hablado sobre este interesante proyecto con
Eduardo Juárez, profesor de la Universidad Politécnica de Madrid y coordinador de NEMESIS-3D-CM, y con Gemma Urbanos, una de las investigadoras más jóvenes implicadas en el mismo.My Scientific Journal. Con vuestro proyecto dais un paso más en el diagnóstico a tiempo real de tumores cerebrales, y en la aplicación de la inteligencia artificial en el campo de la biomedicina, ¿cómo pensáis que podrán llegar a ser los quirófanos en un futuro cercano?Eduardo Juárez y Gemma Urbanos. En las últimas décadas la tecnología en quirófano ha evolucionado considerablemente, habiéndose desarrollado desde material quirúrgico mecanizado hasta tecnologías tan impresionantes como el robot Da Vinci. En el caso de las operaciones de neurocirugía, la incorporación de la resonancia magnética, el microscopio quirúrgico y las herramientas de neuronavegación han supuesto un claro progreso en el método de intervención.El uso de herramientas tecnológicas ayuda al cirujano a operar de forma más segura y efectiva por abordajes más pequeños, por lo que la innovación en el campo de la bioingeniería parece ser el presente y el futuro de la cirugía.

Eduardo Juárez. Coordinador- Profesor Contratado Doctor en UPM
MSCJ. Este proyecto requiere una colaboración muy estrecha de investigadores tanto con cirujanos como con especialistas en anatomía patológica, ¿cómo coordináis toda esta estructura en vuestro grupo de investigación?EJ&GU. Para coordinar este proyecto interdisciplinar en el que colaboramos ingenieros investigadores de la UPM y profesionales de la salud del Hospital 12 de Octubre, trabajamos en tener una comunicación fluida que nos permita intercambiar conocimientos y opiniones, de forma que el proyecto avance de forma conjunta. Además, se han fijado unos objetivos a cumplir en un plazo de tiempo concreto que nos orienta sobre el estado del proyecto. Esto, unido al compromiso de ambas partes, motiva a una colaboración muy enriquecedora.MSCJ. ¿De qué manera puede facilitar el trabajo de los neurocirujanos el desarrollo de este proyecto? ¿En qué áreas específicas puede aportar un avance significativo?EJ&GU. El desarrollo de este sistema médico permitiría al cirujano diferenciar in vivo entre tejido tumoral y tejido sano durante la cirugía, aportando una mayor precisión en la toma de decisiones críticas durante el procedimiento de resección del tumor. 
Gema Urbanos. Investigadora en HU12O
Las distintas áreas en las que el proyecto aporta una propuesta de valor son: la clasificación de diferentes tejidos cerebrales en tiempo real, la creación de un modelo inmersivo 3D del cerebro del paciente y la fusión de las imágenes hiperespectrales con las imágenes de resonancia magnética y ultrasonidos.
MSCJEJ&GU. Clasificar otro tipo de tumores requeriría una nueva investigación donde sería necesario recopilar imágenes hiperespectrales de otros tipos de tumores, y a partir de los datos obtenidos, estudiar cómo se comportan estos tejidos en nuestro modelo. En base a ese estudio, podríamos contestar si es muy difícil o no adaptar los parámetros del algoritmo para clasificar otro tipo de tumores. Sin embargo, las imágenes hiperespectrales han sido ya utilizadas para la detección y diagnóstico de cáncer de cervis, mama, colon, piel, tráquea, ovario, próstata, esófago, lengua y cerebro.
MSCJ. Aunque hoy por hoy trabajáis sobre un prototipo, si finalmente este sistema pudiese desarrollarse de una forma más estandarizada, ¿sería muy complicada su implantación en quirófanos?EJ&GU. La implementación de este sistema en quirófano no es compleja. Se espera que el sistema basado en nuestro prototipo sea una herramienta más con la que el neurocirujano trabaje de forma sencilla e intuitiva, siendo un sistema mucho más económico que otros dispositivos de neuronavegación actual pero ofreciendo además otro tipo de prestaciones.MSCJ. Hablemos de Machine Learning, enseñar a pensar a una computadora. En el proyecto usáis imágenes hiperespectrales contrastadas con valoraciones especializadas, ¿estimáis que se necesitaría un gran número de imágenes hiperespectrales para que el sistema funcione de una forma fiable y con un margen de error pequeño?EJ&GU. Cuantas más imágenes del mismo tipo de tumor cerebral analice el algoritmo, mejores serán los resultados de clasificación, por ello, uno de los objetivos de este proyecto es crear una base de datos con un elevado número de imágenes hiperespectrales durante la cirugía.Documentación y Entrevista
Alba Peña Hidalgo para My Scientific Journal 08/10/2020

Alba Peña HidalgoRedactora My Scientific
Estudiante de Biología

